Într-o decizie stânjenitoare din punct de vedere istoric, FDA a devenit recent singurul organism internațional de reglementare autorizează utilizarea vaccinurilor ARNm de la Moderna și Pfizer pentru copii cu vârsta cuprinsă între șase luni și cinci ani.
Pentru majoritatea covârșitoare a copiilor mici și a copiilor mici, probabil că nu există nicio justificare sau nevoie pentru această autorizație.
Aceștia prezintă un risc extrem de mic de complicații grave din cauza COVID, ceea ce înseamnă că calculul risc-beneficiu este precar în cel mai bun caz și, în cel mai rău caz, potențial negativ.
Este, de asemenea, o dovadă a politizării îngrijorătoare de succes a agențiilor de reglementare din SUA că, în esență, nicio altă țară respectată internațional, nicăieri de pe pământ, nu a luat această decizie uluitoare.
Suedia, de exemplu, are a oprit lansarea a vaccinului Moderna pentru oricine sub 30.
Nu 18. Nu 12. Nu 5. 30.
Statele Unite vor vaccina acum copiii de până la șase luni cu același produs pe care Suedia l-a interzis pentru utilizare oricărei persoane sub 30 de ani, invocând efecte secundare care înclină cifrele risc-beneficiu.
În ciuda acestei diferențe de opinie îngrijorătoare, șeful de cabinet al Casei Albe/președintele interimar Ronald Klain a sărbătorit în mod confuz anunțul:
Interesant, New York Times link Klain pe Twitter a adus în discuție încă un aspect interesant al procesului de autorizare, care necesită o examinare a documentelor FDA și a declarațiilor anterioare.
Prima informație interesantă din lansare îndelungată a FDA este estimarea lor a eficacității vaccinului pentru grupele de vârstă mai înaintate.
Cifrele sunt... sumbre:
Estimările observate ale eficacității vaccinului împotriva bolii simptomatice datorate variantei Omicron includ următoarele: 8.8% (IC 95%, 7.0 până la 10.5) la 25 sau mai multe săptămâni de la vaccinarea primară la adulți; 59.5% în rândul adolescenților cu vârsta cuprinsă între 12 și 15 ani, la 2 până la 4 săptămâni după doza 2, 16.6% în timpul lunii 2 după a doua doză și 9.6% în timpul lunii 3 după a doua doză
8.8% eficacitate împotriva bolilor simptomatice după ~6 luni în rândul adulților.
În doar Două luni de vaccinare, eficacitatea împotriva bolilor simptomatice în rândul copiilor între 12 și 15 ani scade la 16.6% și la 9.6% până în a treia lună. Ei nu specifică eficacitatea după aceea, probabil pentru că scade la zero la sută sau chiar devine negativă.
În plus, estimările lor privind eficacitatea vaccinului împotriva spitalizărilor și vizitelor la departamentele de urgență sunt dramatic mai mici decât ratele de 95-100% susținute de „experți” care au fost folosite pentru a justifica discriminarea și apelurile înfiorătoare pentru a exclude „nevaccinați” de la îngrijirea medicală:
Estimările observate ale eficacității vaccinului ARNm din seria primară împotriva spitalizărilor din cauza variantei Omicron la adulți au fost raportate la 41%-57% la 6-9 luni sau mai mult după a doua doză.
Într-un studiu observațional la adolescenți cu vârsta cuprinsă între 12 și 18 ani (interval median de la vaccinare, 162 de zile) în timpul perioadei predominante Omicron, eficacitatea vaccinului din seria primară a fost de 40% (IC 95%, 9 până la 60) împotriva spitalizării pentru COVID-19.
Estimările observate ale eficacității vaccinului ARNm din seria primară împotriva vizitelor de urgență/îngrijire urgentă din cauza variantei Omicron la adulți au fost raportate între 31%-38% la 6-9 luni sau mai mult după a doua doză.
Indiferent de procentul de eficacitate pretins a fost pre-Omicron, aceste procente sunt mult diminuate în comparație cu așteptările.
Până la 41% pentru eficacitatea vaccinului împotriva spitalizării pentru adulți 6-9 luni sau mai mult după a doua doză.
Departamentul de urgență sau îngrijire de urgență până la 31%. 40% cu un interval de încredere de 9-60% pentru adolescenții cu vârsta între 12-18 ani.
Acesta este încă un motiv pentru care mandatele bazate pe vaccinare sunt complet de neapărat:
Aceste cifre sunt remarcabil de scăzute și ar eșua ținta inițială de 50%. pe care FDA l-a stabilit pentru autorizarea de urgență a vaccinurilor COVID.
Vă amintiți partea îngrijorătoare pe care am menționat-o mai devreme despre procesul pentru copiii mici?
Nu numai că procentele de eficacitate nu ating pragul de 50% la adulți, pentru copii, pur și simplu au renunțat la acel standard.
Pentru a autoriza vaccinul pentru grupele de vârstă mai tinere, FDA a imputat eficacitatea vaccinului prin „imunopunturi” și comparând generarea de anticorpi de la grupele de vârstă mai înaintate:
Eficacitatea vaccinului a fost dedusă prin imunopuntare pe baza unei comparații a obiectivelor de imunogenitate (concentrațiile medii geometrice ale anticorpilor neutralizanți SARS-CoV-2 (GMT) și ratele de răspuns serorespons la 1 lună după doza 3) între participanții cu vârsta de 6-23 de luni din studiul C4591007 (n= 146) și participanții cu vârsta cuprinsă între 16 și 25 de ani din studiul C4591001
În esență, chiar dacă crearea de anticorpi nu este în mod clar suficientă pentru a preveni infecția simptomatică sau pentru a atinge estimările inițiale de 95%, FDA a dedus eficacitatea vaccinării în rândul bebelușilor și copiilor mici pe baza comparațiilor cu generarea de anticorpi.
În acest moment, este deja evident de ce SUA va fi singura țară occidentală care va începe vaccinarea ARNm pentru copiii atât de tineri.
Presiunea politică din partea președintelui interimar Klain, a activiștilor precum Ashish Jha, Jeremy Faust, Jerome Adams și alții este incontestabil periculoasă.
Acest lucru ar putea explica de ce FDA a schimbat obiectivul de la 50% eficacitate la generarea de anticorpi - să se supună presiunii politice din partea Casei Albe și a aliaților lor din mass-media și comunitatea de „expert”.
Luna trecută, Vinay Prasad a detaliat absurditatea acestei decizii:
El mai menționează că ținta de 50% stabilită inițial a fost „arbitrară” și destul de scăzută.
Eficacitatea vaccinărilor împotriva spitalizării în epoca Omicron pentru cei care sunt „complet vaccinați” este LOWER decât atât, și au dedus eficacitatea în rândul copiilor mici pe baza generării de anticorpi din aceleași grupuri de vârstă.
Pe scurt, ei și-au aruncat ținta determinată în mod arbitrar, care era deja scăzută, și apoi au imputat eficacitatea pe baza unui punct final (generarea de anticorpi) despre care am văzut deja că nu funcționează deosebit de bine față de varianta dominantă actuală.
Deci sigur, acest lucru este extrem de deconcertant și frustrant, dar hei, cel puțin Ron Klain este fericit.
Imunitatea naturală
FDA, în înțelepciunea lor infinită, a ignorat, de asemenea, că propriile estimări ale CDC, care afirmă că 75% dintre copii au avut deja COVID:

Desigur, nimeni implicat în acest proces de luare a deciziilor nu este dispus să recunoască că 75% dintre copii au fost infectați cu COVID, în ciuda mascării, închiderii școlilor și a altor „intervenții” menite să prevină sau să „încetinească” răspândirea virusului. Dar mă abat.
Imunitatea naturală este probabil mai protectoare împotriva infecțiilor viitoare decât vaccinarea, așa cum explică acest tweet Tracy Høeg pe baza datelor dintr-un studiu New England Journal of Medicine:
FDA s-a întrebat pentru a autoriza vaccinurile pentru copiii extrem de mici pe baza răspunsului anticorpilor în loc de estimări de eficacitate, ignorând, în același timp, faptul că 75% dintre copiii mici aveau deja o protecție mai bună.
Este o clinică în ce să nu faci.
Estimări efective de eficacitate
FDA a generat unele estimări ale eficacității vaccinului atât pentru vârstele 6-23 luni, cât și 2-4 ani, iar cifrele la care au ajuns arată de ce au trebuit să recurgă la răspunsul cu anticorpi în loc de reducerea efectivă dovedită.
Participanți cu vârsta cuprinsă între 6-23 de luni
O analiză descriptivă preliminară a eficacității a cazurilor de COVID-19 care au apărut la cel puțin 7 zile după doza 3 în rândul participanților cu vârsta cuprinsă între 6-23 de luni din populația cu eficacitate evaluabilă din doza 3 a inclus un total de 3 cazuri confirmate acumulate la participanți cu și fără dovezi de anterioare. Infecția cu SARS-CoV-2 până la limita de date din 29 aprilie 2022. Populația cu eficacitate evaluabilă pentru doza 3 a inclus 376 de participanți randomizați la BNT162b2 și 179 de participanți randomizați la placebo. Estimarea VE în această analiză preliminară a fost de 75.6% (IC 95%: -369.1%, 99.6%), cu 1 caz COVID-19 în grupul BNT162b2 comparativ cu 2 în grupul placebo (randomizare 2:1 BNT162b2 la placebo).
Subliniere adăugată
A fost 1 caz în grupul de vaccinare și 2 în grupul placebo. Asta e.
Așa se ajunge la intervale de încredere de la -369.1% la 99.6%. Vaccinul ar putea avea o eficacitate negativă de aproape 400% pentru bebeluși sau ar putea fi unul dintre cele mai bune vaccinuri create vreodată cu o eficacitate aproape perfectă. Cine ştie! Cu siguranță nu FDA pe baza a 3 cazuri totale de COVID în această grupă de vârstă.
Dar nu vă faceți griji, au colectat mult mai multe date pentru grupa de vârstă 2-4 ani.
Setul de date a avut un total de 7 cazuri:
Participanți cu vârsta cuprinsă între 2-4 ani
O analiză descriptivă preliminară a eficacității a cazurilor de COVID-19 care au apărut la cel puțin 7 zile după doza 3 în rândul participanților cu vârsta de 2-4 ani din populația cu eficacitate evaluabilă în doza 3 a inclus un total de 7 cazuri confirmate acumulate la participanți cu sau fără dovezi de anterioare.
Infecția cu SARS-CoV-2 până la data limită de date din 29 aprilie 2022. Populația cu eficacitate evaluabilă pentru doza 3, cu și fără dovezi de infecție anterioară cu SARS CoV-2, a inclus 589 de participanți randomizați la BNT162b2 și 271 de participanți randomizați la placebo. Estimarea VE în această analiză preliminară a fost de 82.4% (IC 95%: -7.6%, 98.3%), cu 2 cazuri de COVID-19 în grupul BNT162b2 comparativ cu 5 în grupul placebo (randomizare 2:1 BNT162b2 la placebo). Un caz confirmat în grupul placebo a apărut la un participant cu dovezi de infecție cu SARS-CoV-2 înainte de 7 zile după doza 3.
Ei bine, măcar suntem la o posibilă eficacitate negativă de 8% în intervalele de încredere!
Dar din nou, nu vă faceți griji, FDA este conștientă de această limitare și de multe altele în afară de:
Într-o analiză combinată a ambelor grupe de vârstă, VE a fost de 80.4% (IC 95%: 14.1%, 96.7%), cu 3 cazuri în grupul BNT162b2 și 7 cazuri în grupul placebo. Interpretarea datelor de eficacitate post-doza 3 pentru ambele grupe de vârstă și pentru grupa de vârstă de 6 luni până la 4 ani în general, este limitată din următoarele motive:
- Eficacitatea vaccinului după doza 3 nu poate fi estimată cu precizie din cauza numărului limitat de cazuri acumulate în timpul urmăririi în orb, așa cum se reflectă în intervalele largi de încredere asociate cu estimările.
- Aceste date descriptive privind eficacitatea sunt preliminare, deoarece protocolul a specificat 21 de cazuri nu au fost încă realizate.
- Au existat intervale de dozare foarte variabile între dozele 2 și 3, cu intervale mediane de 112 (interval 56 până la 245) zile în rândul participanților cu vârsta de 6-23 luni și 77 (interval 42 până la 239) zile în rândul participanților cu vârsta de 2-4 ani în populația cu eficacitate evaluabilă în doza 3.
- Timpul median de urmărire în orb după doza 3 în analize a fost de numai 35 de zile pentru participanții cu vârsta cuprinsă între 6 și 23 de luni și de 40 de zile pentru participanții cu vârsta cuprinsă între 2 și 4 ani.
Protocolul prevedea că 21 de cazuri nu au fost realizate. Dar au autorizat vaccinurile oricum!
În grupul de vârstă 2-4 ani, a existat o rată semnificativ mai mare de cazuri care „îndeplinesc criteriile pentru COVID-19 sever” în grupul care a primit vaccinul:
Șapte cazuri la participanții cu vârsta de 2-4 ani au îndeplinit criteriile pentru COVID-19 sever: 6 în grupul BNT162b2, dintre care 2 cazuri au avut loc după deblocare și 1 în grupul placebo.
Acest lucru nu înseamnă că cei care se vaccinează sunt mai mult probabil să aibă un caz sever de COVID, dar subliniază încă o dată problema unor dimensiuni atât de mici ale eșantioanelor și abandonării țintelor inițiale.
Și trebuie remarcat faptul că cazurile grave au fost determinate a nu fi „semnificative clinic:”
Toate acestea au fost considerate de către investigator ca nesemnificative clinic pe baza examinării la vizita la boală și a circumstanțelor contributive, cum ar fi plânsul participantului în timpul examinării
Tabelele de date
FDA știe că majoritatea americanilor nu se vor uita niciodată la tabelele de date, în special pe cei din media și activiștii din clasa „expert” pe Twitter.
Dar oricine le examinează poate înțelege imediat absurditatea procesului de luare a deciziilor FDA:
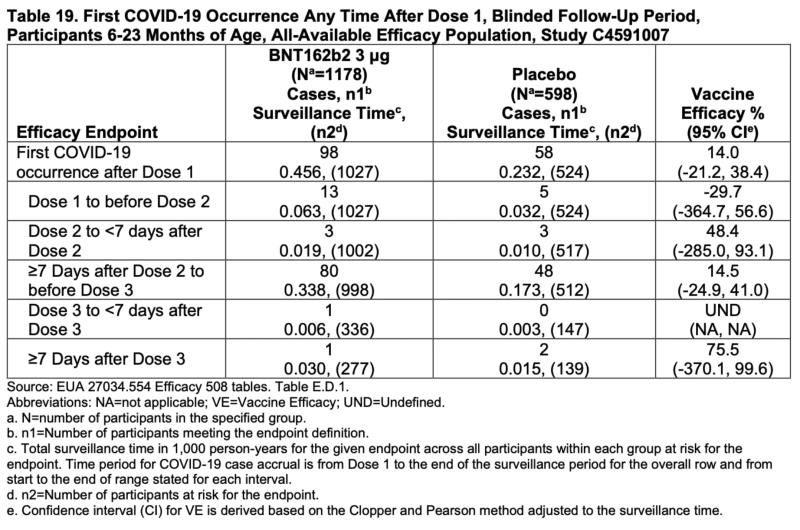
Intervalele de încredere pentru fiecare calcul al eficacității pentru participanții 6-23 de luni scad sub zero. Fiecare singur.
Estimarea globală este de 14% și chiar și asta ar putea fi chiar și la -21.2%.
E doar de râs. Ei bine, ar fi de râs dacă nu ar fi o decizie atât de importantă.
Dacă vrei să fii caritabil, cel puțin procentul general de eficacitate pentru cei cu vârsta cuprinsă între 2 și <5 nu a avut intervale de încredere negative:
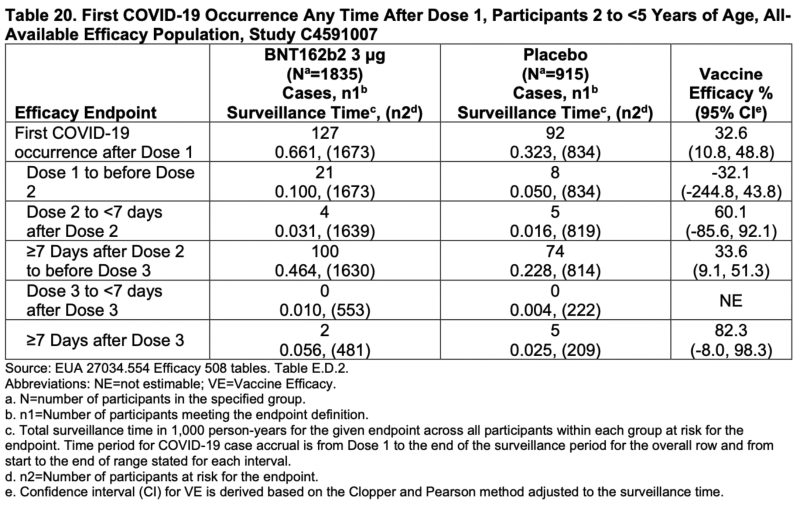
Deși trei dintre cele patru obiective principale au avut intervale de încredere negative, deci necesită încă o cantitate semnificativă de caritate.
De asemenea, este de remarcat faptul că perioada de timp dintre administrarea dozei 1 și a dozei 2 a fost asociată cu eficacitate negativă în ambele grupe de vârstă.
Acest lucru a contribuit probabil la probleme de raportare a datelor atunci când se calculează eficacitatea vaccinului în lumea reală. Orice caz care apare în această perioadă este considerat „nevaccinat”, cu excepția acestor grupe de vârstă, când eficacitatea este la cel mai scăzut punct.
Faptul că FDA a autorizat aceste vaccinuri pentru copii pe baza acestor date este pur și simplu de neiertat.
Dimensiunile eșantionului nu au îndeplinit protocolul specificat pentru 21 de cazuri.
Calculele eficacității vaccinului, chiar și excluzând intervalele de încredere gigantice, au fost cu mult sub ținta arbitrară de 50% pe care au creat-o pentru autorizarea utilizării de urgență în rândul adulților.
Includerea intervalelor de încredere arată posibilitatea unei eficacități negative, care, deși este puțin probabilă, este încă posibilă având în vedere numărul extraordinar de mic de cazuri atât în grupul vaccin, cât și în grupul placebo.
Ei au folosit pur și simplu „imunopuntura” pentru a deduce protecția bazată pe generarea de anticorpi, în loc de rate de eficacitate predeterminate.
Este încă un indicator terifiant al cât de motivată politic a devenit FDA și al modului în care activismul a distorsionat onestitatea intelectuală.
„Experții” sunt atât de disperați să-și mențină reputația și să evite să fie etichetați ca „anti-vaxxer” de către influenți precum Eric Feigl-Ding, Angela Rasmussen și alții, încât par să nu fie dispuși să semnaleze defecte în procesul de luare a deciziilor.
În același timp, este greu și ușor de crezut că asta a fost tot ce a fost nevoie pentru a justifica o vaccinare „de urgență” pentru grupuri de vârstă cu risc extrem de scăzut de îmbolnăvire severă.
Această decizie va fi, pe bună dreptate, un alt motiv pentru erodarea din ce în ce mai mare a încrederii în presupușii „experți” ai sănătății publice, o jenă pentru autoritățile de reglementare din SUA capturate de politică.
Publicat sub a Licență internațională Creative Commons Attribution 4.0
Pentru retipăriri, vă rugăm să setați linkul canonic înapoi la original Institutul Brownstone Articol și autor.










